Onderzoeker van de week: Victor Peperzak

3 keer Alpe-onderzoek
In de afgelopen jaren hebben de deelnemers van de Alpe d’HuZes miljoenen euro’s opgehaald voor de bestrijding van kanker. Daarmee zijn honderden slimme onderzoekers aan het werk gezet. Onder hen dr. Victor Peperzak: hij begint dit jaar alweer aan zijn derde Alpe-onderzoeksproject, een unicum. In 2015 won hij als jonge onderzoeker de Bas Mulder Award. In 2017 kwam er een nieuw project bij, en dit jaar start hij met een ‘Uniek hoogrisicoproject’ waarin hij op unieke wijze kankercellen om zeep hoopt te helpen. De Alpe loopt als een rode draad door zijn carrière, waarover hij uitgebreid vertelt.
Waarom is jouw onderzoek eigenlijk zo populair bij de Alpe d’HuZes?
“Ik werk met mijn onderzoeksgroep in het UMC Utrecht aan een aantal ongeneeslijke vormen van kanker. Het gaat om hematologische kankers, bloedkanker. Voor deze vorm van kanker is kennis van het immuunsysteem belangrijk en dat is precies mijn achtergrond. Ik ben daarin getraind bij het Nederlanders Kanker Instituut en in het buitenland. Daardoor ken ik het immuunsysteem van binnen en buiten. Ik ben eigenlijk van daaruit het kankeronderzoeksveld ingerold en spits mijn kennis nu toe op de hematologische kankers. Daar is nog ontzettend veel winst te boeken. Er zijn door de jaren heen veel medicijnen en mogelijkheden ontwikkeld, alleen werkt het nog niet altijd even goed.”
Het gaat jou dus niet om het ontwikkelen van nieuwe geneesmiddelen?
“Er zijn al heel veel geneesmiddelen. We willen deze combineren en de beste combinaties vinden om deze kankers beter te kunnen behandelen. Dit doen we niet door ze willekeurig bij elkaar te gooien natuurlijk. In het laboratorium behandelen we kankercellen met een van deze middelen. Als de cel dat overleeft bekijken we hoe het kan dat die cel resistent is. En of we die resistentie weer kunnen remmen met een ander middel.”
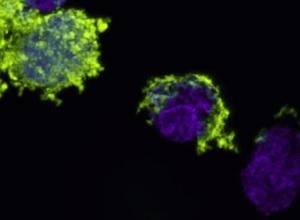
Kankercellen (waarvan de celkern in paars) met daarin een zelf ontwikkeld giftig molecuul (geel) dat door aangepaste T cellen specifiek in kankercellen kan worden gepompt.
(Foto: Victor Peperzak)
Wat maakt jouw onderzoek uniek?
“De unieke positie die we hier hebben is dat we heel goed onderzoek met patiëntenmateriaal kunnen doen. We hebben een goede samenwerking met hematologen waardoor we makkelijk materiaal kunnen verkrijgen. Vervolgens kunnen we die samples heel goed opkweken met zelf ontwikkelde methoden. We kweken de kankercellen in een soort 3D-gel, waarin we de leefomgeving van de kankercellen, namelijk het beenmerg, goed kunnen nabootsen.”
Hoe moet ik dat zien? Als een soort haargel?
“Ja, inderdaad. Je kent waarschijnlijk organoids wel: dat zijn ook gekweekte tumorcellen, maar dan in een mini-orgaantje of klompje met cellen. Voor de tumoren waar ik aan werk, kun je niet van die klompjes maken. Het zijn losse cellen. Daarom kweken we ze in hun 3D-context, in een gel. Het is een heel mooi systeem om kankercellen in te onderzoeken. De cellen gedragen zich namelijk net als in het lichaam. We kunnen bijvoorbeeld cellen aan die gel toevoegen die dezelfde signalen geven als de cellen in het beenmerg van een patiënt doen. Zo maken we de omgeving voor die kankercellen zo natuurlijk mogelijk.”
Nu is de tijd om dit soort dingen goed te doen.
En wat onderzoek je dan in die gel?
“We kweken de kankercellen in die gel, behandelen ze met middel A, bekijken welke cellen doodgaan en welke niet. Van de cellen die niet doodgaan bekijken we waaróm dat zo is. Er zijn veel middelen beschikbaar, dus bekijken we of we die cellen daar alsnog mee dood kunnen maken. Het is eigenlijk heel simpel, maar het is natuurlijk wel veel werk om te doen.”
Als ik het zo hoor is dit een perfect tijdperk om onderzoek in te doen.
“Ja, want hoe simpel het ook klinkt: dit onderzoek kan nu pas goed gedaan worden. Die cellen kun je normaalgesproken helemaal niet kweken, die zijn binnen een dag dood. Nu kan het wel, in een modelsysteem die sterk nabootst op wat er in de patiënt gebeurt. Nu is de tijd om dit soort dingen goed te doen.”
Je hebt nu het onderzoeksproject beschreven waarvoor je in 2017 financiering hebt gekregen. Vloeit dat voort uit de Bas Mulder Award die je in 2015 kreeg?
“Ja klopt. Al loopt dat project ook nog. Het ging destijds om een 6-jarig programma, daarvan zijn er nu nog 3,5 te gaan. In dat onderzoek richten we ons op de celdood van kankercellen. Er is een familie van eiwitten die het zelfmoord plegen (apoptose) van cellen reguleert. Dat is een heel natuurlijk proces: cellen met stress hóren zelfmoord te plegen. Dat gebeurt constant in je lichaam, anders zat je vol met tumoren. Maar: kankercellen hebben dat proces uitgeschakeld. Wij onderzoeken in dat project hoe dat nou gaat. En we hebben ook al resultaten. Er is een eiwit, MCL-1, dat het doodgaan van cellen remt. We vroegen ons af of je dat eiwit op zijn beurt weer kunt remmen. Maar daarbij dachten we wel: ‘dit eiwit is zó essentieel voor gezonde cellen, dat moet je niet overal remmen, want dan maak je meer kapot dan je lief is’. Dus zochten we een manier om het eiwit heel specifiek in kankercellen te remmen. We hebben nu gevonden dat er moleculen zijn, fosfatasen, die de hoeveelheid van dit eiwit bevorderen in kankercellen. Als je die fosfatasen remt, zie je ook dat die eiwitten worden geremd. Maar: alleen in kankercellen, niét in de gezonde cellen.”
Ik heb vooral dankzij financiering van de Alpe nu een onderzoeksgroep met 7 mensen samen kunnen stellen.
Dan nu het meest recente project, het Uniek hoogrisicoproject. Dat is weer even heel wat anders, he?
“Klopt ja, dat gaat over de rol van T-cellen in het immuunsysteem. Immunotherapie is heel erg ‘booming’, het heeft veel potentie. Maar wat we ook zien, is dat het voor sommige tumoren goed werkt, maar de resultaten bij andere tumoren achterblijven. T-cellen kunnen kankercellen doden. Dat doen ze door een giftige stof in kankercellen te pompen. Maar er zijn kankercellen die daar op hun beurt remmers voor hebben. Wij willen daarom proberen de T-cellen te voorzien van een krachtiger mechanisme: een nóg giftiger molecuul waarvoor de kankercellen géén remmers hebben. Dat is een unieke aanpak: er wordt wereldwijd veel gesleuteld aan T-cellen, maar puur het verbeteren van die toxische rol? Voor zover wij weten zijn we daarin uniek.”
Wat houdt zo’n Uniek hoogrisicoproject verder in?
“Waar het om gaat, is dat je een idee hebt dat in theorie heel goed werkt. Maar is dat in de praktijk ook zo? Dat willen we in dit verkorte traject uitzoeken. Aan het eind moet duidelijk zijn of het de potentie heeft voor vervolgonderzoek.”
Je hebt nu 3 projecten uitgelegd. Hoe ‘switch’ je tussen die projecten in een gemiddelde werkweek?
“Ik heb vooral dankzij financiering van de Alpe nu een onderzoeksgroep met 7 mensen samen kunnen stellen, die op de verschillende projecten werken. De projecten lopen dus continu door, het is niet de ene dag het ene project en de andere dag het andere project. Ik sta zelf niet meer in het lab, dat is wel eens jammer. Toen ik hier begon dacht ik: ‘Ik ga het 50/50 doen. De helft van de tijd sta ik op het lab en de andere helft ben ik manager van de groep.’ Maar dat werkt niet. Het is een ‘dedicated’ beroep, je kunt niet af en toe een aantal uren op het lab staan. Maar ik loop er uiteraard nog wel rond en overleg veel over de voortgang en knelpunten van de projecten. Ik ben wel voor de volle 100% bezig met onderzoek.”
Als training heb ik alle trappenhuizen op het AMC heen en weer gelopen. Zwaar, maar een goede voorbereiding!
Je Bas Mulder Award nam je in 2015 in ontvangst op de berg. Hoe was dat voor je?
“De sfeer vond ik vooral heel goed. Ik kreeg mijn prijs op een podium. Daarna ging ik naar een café, waar mensen me herkenden, een biertje kwamen brengen en hun persoonlijke verhaal vertelden. Het was emotioneel, maar ook echt hartverwarmend. Zelf deed ik dat jaar ook mee, niet als fietser, maar als hardloper. Ik hoorde pas een aantal weken van tevoren dat ik erheen mocht, dus dat was wel even flink aanpoten. Als training heb ik alle trappenhuizen op het AMC -waar ik toen werkte- heen en weer gelopen. Zwaar, maar een goede voorbereiding!”
Laatste vraag. Stel dat de Alpe-deelnemers dit jaar 50 miljoen euro bij elkaar brengen en de organisatie besluit dat dit geheel ter beschikking van jouw onderzoek komt. Wat ga je er dan mee doen?
“Ik kijk nu puur naar een aantal specifieke hematologische kankers, dat heeft te maken met het aantal handjes dat we hebben. Daarin moeten we keuzes maken. Met meer handjes kunnen we ook naar meer vormen van kanker kijken. En ook dat Uniek hoogrisicoproject: daar is zóveel werk in te verrichten als dat slaagt. Nu is het nog heel klein, maar ik zie voor me dat we het daadwerkelijk kunnen testen in meerdere tumoren, in 3D-kweken en organoïds… we hopen het bij veel meer typen tumoren in te kunnen zetten.”


